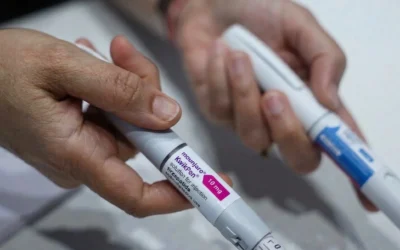
Ministerul Sănătății analizează posibilitatea eliberării medicamentului FAVIPIRAVIR în ambulatoriu, prin farmaciile cu circuit închis din cadrul spitalelor, cu prescripție medicală, la recomandările specialiștilor din Comisia de specialitate de boli infecțioase.
În acest moment, pentru acest medicament, Agenția Națională a Medicamentului și Dispozitivelor Medicale din România a realizat o evaluare în baza căreia a emis o autorizaţie pentru nevoi speciale valabilă în România și în baza căreia se permite administrarea în unitățile sanitare, sub supraveghere medicală, având o utilizare restrictivă.
Astfel, în India, țara de proveniență, FAVIPIRAVIR are un aviz temporar pentru fabricaţie şi comercializare obținut în urma unui proces de evaluare accelerată și conditionată de multiple cerințe și care nu poate fi asimilată cu o autorizație de punere pe piață emisă în acord cu legislația europeană în vigoare.
“După discuțiile avute cu specialiștii din Comisia de boli infecțioase și conducerea Agenției Naționale a Medicamentului, vom studia posibilitatea eliberării acestui medicament în ambulatoriu prin farmaciile de circuit închis din cadrul spitalelor, gratuit, numai cu prescripție medicală și cu urmărirea bolnavului pe parcursul tratamentului de către medicul de familie”, a precizat dr. Andrei Baciu, secretar de stat în Ministerul Sănătății.
Potrivit Protocolului Național de tratament al bolnavilor infectați cu virusul SARS-Cov-2, medicamentul FAVIPIRAVIR este recomandat a fi administrat în formele ușoare și medii de infecție cu noul corornavirus în prima săptămână de boală.
Astfel, într-o adresă către Ministerul Sănătății, Comisia de specialitate de boli infecțioase crede că medicamentul poate fi eliberat în spital și ambulatoriu la recomandarea medicilor, numai cu prescrispție medicală.
De asemenea, referitor la profilul de siguranță din datele preliminare disponibile, FAVIPIRAVIR prezintă un risc de teratogenicitate și risc de afectare hepatică.